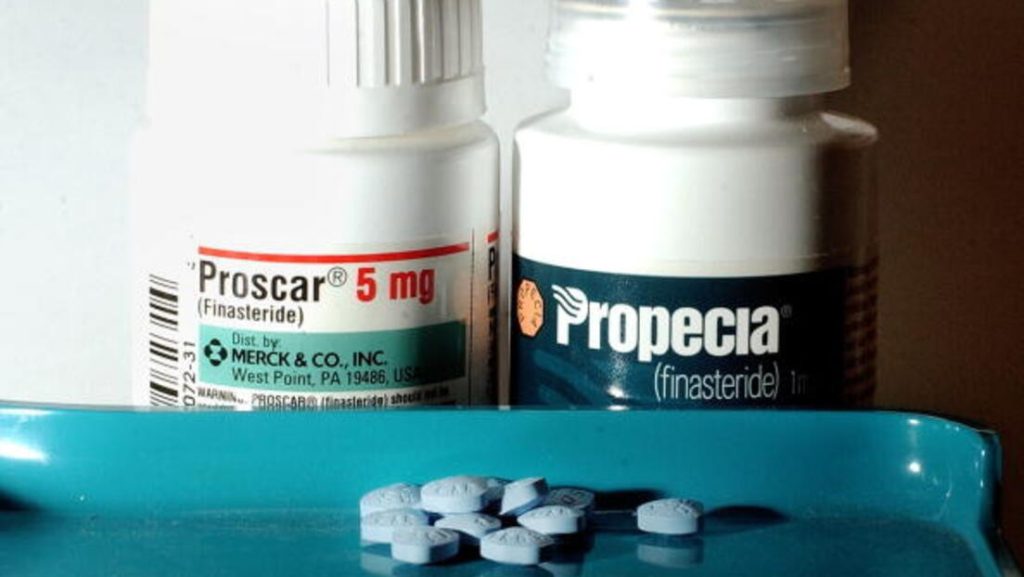
Fármacos.
Una investigación publicada el mes pasado en la Revista de Psiquiatría Clínica sostiene que el finasteride, medicamento utilizado por millones de personas para tratar la calvicie masculina, estaría asociado a un incremento significativo de trastornos del ánimo y pensamientos suicidas.
El estudio fue dirigido por Mayer Brezis, del Centro Médico Hadassah-Hebrew University (Israel), quien aseguró que “la evidencia ya no es anecdótica” y que los patrones observados son “consistentes” en distintas poblaciones. “Y las consecuencias podrían haber sido trágicas”, afirmó.
La investigación abarca datos de ocho estudios realizados entre 2017 y 2023 que se basaron en los sistemas de datos de varios países, incluido EE.UU., y en registros sanitarios nacionales de Suecia, Canadá e Israel.
Los hallazgos de estos estudios muestran un patrón consistente entre quienes recurrían al uso del finasteride, siendo más propensos a tener una probabilidad significativamente mayor de experimentar trastornos del estado de ánimo y pensamientos suicidas que aquellos que no tomaban el fármaco.
El finasteride, aprobado por la Administración de Alimentos y Medicamentos de EE.UU. (FDA) en la década de 1990 y comercializado por la farmacéutica Merck bajo el nombre Propecia, ya tenía antecedentes de advertencias. En 2011, la FDA agregó la depresión como posible efecto adverso, y en 2022, la ideación suicida. Sin embargo, Brezis reveló que existían recomendaciones internas desde 2010 para incluir esos riesgos en la etiqueta, que fueron rechazadas sin explicación pública.
Según el artículo, cientos de miles de personas pueden haber sufrido depresión relacionada con el finasteride, y cientos, o posiblemente más, pueden haber muerto por suicidio.
El investigador afirma haber encontrado documentos confidenciales de la FDA con secciones censuradas y registros de al menos 18 suicidios vinculados al fármaco en 2011, aunque estima que la cifra real podría ser de “miles” en todo el mundo debido a un “fallo sistémico de farmacovigilancia”. Además, acusó a Merck de haber omitido investigaciones básicas de seguridad y a las autoridades regulatorias de no haber exigido los estudios posteriores a la aprobación.
Ante estos hallazgos, Brezis pidió suspender el uso cosmético del finasteride hasta completar una nueva evaluación de seguridad y exhortó a la FDA a garantizar controles más estrictos sobre los efectos psiquiátricos de los medicamentos. Tanto la agencia estadounidense como Merck fueron contactadas por The New York Post para pedir su versión, pero no respondieron.